上海泉众机电科技有限公司
8 年
手机商铺
商家活跃:
产品热度:
- NaN
- 0.7000000000000002
- 1.7000000000000002
- 0.7000000000000002
- 3.7
流体剪切力刺激内皮细胞与平滑肌细胞共培养系统
询价
推荐产品
公司新闻/正文
Asprosin 通过脂肪细胞和巨噬细胞共培养增强细胞因子的产生,导致肥胖相关炎症的恶化
968 人阅读发布时间:2024-05-27 10:09
白脂素(Asprosin)是一种新型脂肪细胞因子,主要由禁食期间白色脂肪组织中的脂肪细胞分泌,能够快速诱导生成葡萄糖并且调控肝脏中葡萄糖的释放。据报道,在饮食诱导的肥胖者中也观察到由 Asprosin 刺激的葡萄糖产生。在正常情况下,这种分子的活性有助于通过调节食欲和葡萄糖分泌来维持适当的能量稳态。此外,一些研究表明,在肥胖个体以及胰岛素抵抗和1型糖尿病(DM1)或2型糖尿病(DM2)的患者中观察到其病理性升高水平。然而,人们对 Asprosin 作用机制知之甚少,特别是在关键胰岛素敏感组织(骨骼肌和胰腺β细胞)中诱导炎症以及通过激活促炎机制加剧组织损伤的机制方面。
研究表明,Asprosin 在高血糖条件下通过激活与 TLR4 通路相关的促炎机制来损害胰腺β细胞的胰岛素分泌。研究还发现,Asprosin 通过产生内质网应激和诱导促炎因子来降低骨骼肌胰岛素敏感性,并通过激活 IKKβ-NF-κBp65 通路增强肥胖个体中高脂血症诱导的内皮炎症。然而,迄今为止,没有证据表明 Asprosin 直接或间接负责调控脂肪细胞功能,导致肥胖相关炎症。但是,它在肥胖中的显著升高水平和相关的组织损伤增强,以及胰腺和骨骼肌中促炎反应的激活表明,它至少部分参与了中度肥胖相关炎症的调控。
因此,波兰雅盖隆大学生物力学和运动机能学系的一项研究旨在确定 Asprosin 是否对模拟肥胖相关炎症状态的脂肪细胞-巨噬细胞共培养系统中的中度炎症过程具有调节作用,同时确定成熟脂肪细胞(即脂肪细胞的肥大)是否影响 Asprosin 作用的性质。研究成果发表在 International Journal of Molecular Sciences 期刊题为“Asprosin Enhances Cytokine Production by a Co-Culture of Fully Differentiated Mature Adipocytes and Macrophages Leading to the Exacerbation of the Condition Typical of Obesity-Related Inflammation”。

为了研究 Asprosin 对中度肥胖相关炎症发展的影响,研究人员选用小鼠 3T3-L1 前脂肪细胞和 RAW264.7 巨噬细胞为实验细胞株,体外培养 3T3-L1 前脂肪细胞诱导分化为成熟脂肪细胞,然后构建脂肪细胞和巨噬细胞的共培养。考虑到脂肪细胞的分化阶段和成熟度以及脂滴沉积的影响,在分化 7、14 和 21 天后进行评估。首先,评估了 Asprosin 对不同分化阶段细胞共培养物的整体活力和活性的影响。结果表明,Asprosin(0-100 nM)对分化第 7、14 和 21 天的细胞活力和整体活性没有影响。
然后,在有和没有脂多糖(LPS)刺激的共培养物中评估了 Asprosin 对关键促炎细胞因子(如 TNF-α、IL-1β、IL-6和 HMGB1)表达和释放强度的影响。结果表明,单独使用Asprosin 对所分析细胞因子的表达和释放没有影响,仅在进行 LPS 刺激时观察到效果。在不完全成熟细胞(LPS刺激)共培养物(第14天)中,Asprosin 不调节关键炎症细胞因子的表达和释放。然而,在较高浓度的 Asprosin下,在低成熟度共培养物(第 7 天)中,主要促炎细胞因子(即 TNF-α、IL-6 和 HMGB1)的表达和释放强度与 LPS 刺激的共培养物相比降低。
当 Asprosin 作用于含有完全分化和成熟脂肪细胞的 LPS 刺激的共培养物时,观察到不同的效果(第21天)。最高浓度的Asprosin(100 nM)导致促炎 TNF-α,IL-6,IL-1β(图1)和 HMGB1 细胞因子的升高。在 mRNA 水平上的表达分析表明,细胞因子释放的增加取决于这些细胞因子在巨噬细胞和脂肪细胞中表达的增强(图1)。值得注意的是,Asprosin 在巨噬细胞中的作用似乎比在脂肪细胞中更明显,巨噬细胞中的细胞因子表达水平远高于脂肪细胞。此外,促炎因子在脂肪细胞-巨噬细胞共培养物中的表达明显高于脂肪细胞和巨噬细胞的单培养,表明这些细胞在共培养中的合作具有显著的累加效应。这些观察结果证实,构建脂肪组织并参与肥胖相关炎症发展的两个细胞群都对 Asprosin 的作用敏感,Asprosin 作为促炎激活因子作用于它们。
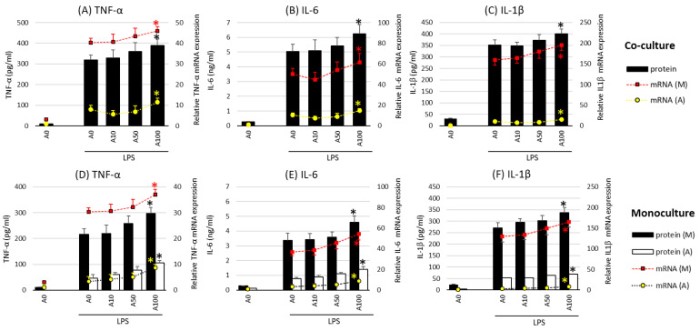
图1 Asprosin 对脂多糖(LPS,100 ng/mL)诱导的细胞因子 mRNA 表达和释放的影响:分化的第 21 天,在脂肪细胞-巨噬细胞共培养物(上)中肿瘤坏死因子-α(TNF-α)(A)、白细胞介素-6(IL-6)(B)和白细胞介素-1 β(IL-1β)(C),和在脂肪细胞和巨噬细胞单一培养物(下)中 TNF-α(D)、IL-6(E)和 IL-1β(F)。
Asprosin 对瘦素和脂联素(关键的脂肪因子)释放的影响取决于脂肪细胞的成熟程度。在共培养的第7天和第14天,无论 LPS 是否刺激,Asprosin 都没有影响这两种脂肪因子在 mRNA 和蛋白质水平上的释放。然而,高浓度 Asprosin 作用于成熟的 LPS-刺激的共培养物和脂肪细胞单培养物均降低了抗炎脂联素的释放,同时瘦素的释放略有增加。这种效应在脂联素的 mRNA 和蛋白质水平上都很明显(图2)。与关键促炎细胞因子的释放一样,脂肪细胞单培养中脂肪因子的水平低于共培养水平,这可能表明巨噬细胞的累加相互作用。
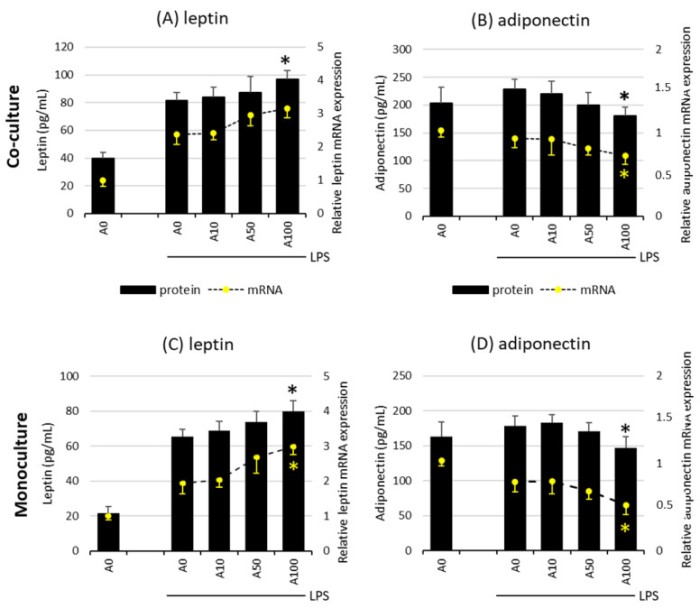
图2 Asprosin 对 LPS(100 ng/mL)诱导的瘦素表达和释放(A)或脂联素表达和释放(B)的影响在分化 21 天时脂肪细胞-巨噬细胞共培养物中,以及瘦素表达和释放(C)或脂联素表达和释放(D)在分化 21 天时脂肪细胞单培养物中。
最后,实验评估了 Asprosin 对巨噬细胞流入脂肪组织的影响,这是由脂肪组织中细胞释放的趋化因子的活性引起的。巨噬细胞与肥胖相关的中度炎症的发展相关。为此,研究了巨噬细胞向脂肪细胞培养物迁移的上清液。
结果表明,Asprosin 通过作用于成熟的脂肪细胞培养物来影响巨噬细胞释放的趋化因子和迁移。高剂量的 Asprosin 显著增加了巨噬细胞在第 21 天从培养物向共培养物和脂肪细胞上清液的迁移程度,但在第 7 天或第 14 天没有从培养物中迁移(图3 A)。这表明,Asprosin 增加巨噬细胞向培养的成熟肥大脂肪细胞的迁移。这种迁移活性的增加与巨噬细胞主要趋化因子 MCP-1 的表达和释放增加相对应(图3 B)。在培养第7天,注意到 MCP-1 表达略有下降,然而,这并没有被趋化因子本身释放减少或巨噬细胞内流减少所证实。此外,如前所述,MCP-1 在巨噬细胞中的表达明显高于脂肪细胞(图3 B)。因此,Asprosin 对巨噬细胞的影响比对脂肪细胞的影响更强烈。然而,没有观察到 Asprosin 对巨噬细胞内流和无 LPS-处理的细胞释放的 MCP-1 水平的影响。可能在肥胖状态下,其升高的水平可能会增加免疫活性细胞涌入脂肪组织,从而增强组织的促炎活化。
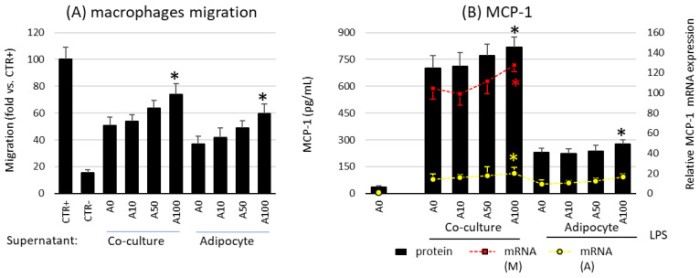
图3 (A)Asprosin 对在不同 Asprosin 浓度(0、10、50 或 100 nM)下培养 24 小时(分化 21 天后)的RAW 264.7 巨噬细胞迁移到从共培养物或脂肪细胞中收集的条件培养基中的影响。(B)脂肪细胞-巨噬细胞共培养物或脂肪细胞培养物中Asprosin 对脂多糖(LPS)诱导的单核细胞趋化蛋白1(MCP-1)mRNA 表达和释放的影响。
总之,这项研究首次利用脂肪细胞和巨噬细胞的共培养评估了 Asprosin 对肥胖相关疾病典型炎症激活的影响。这项研究使我们能够确定与肥胖相关的炎症是否至少一定程度上与 Asprosin 的活性有关,Asprosin 的浓度在肥胖人群中增加。根据获得的结果,可以得出结论,Asprosin 作为从肥胖个体的脂肪组织释放的生物分子,可以被认为是具有潜在促炎作用的免疫调节因子。Asprosin 不仅可能调节食物摄入,还可能通过发展中度肥胖相关的炎症与肥胖相关疾病的病理机制有关。
参考文献:Mazur-Bialy AI. Asprosin Enhances Cytokine Production by a Co-Culture of Fully Differentiated Mature Adipocytes and Macrophages Leading to the Exacerbation of the Condition Typical of Obesity-Related Inflammation. Int J Mol Sci. 2023 Mar 17;24(6):5745. doi: 10.3390/ijms24065745. PMID: 36982813; PMCID: PMC10056564.
原文链接:https://pubmed.ncbi.nlm.nih.gov/36982813/
图片来源:所有图片均来源于参考文献
本文旨在分享、交流生物领域研究进展,进入官网www.naturethink.com或关注“Naturethink”公众号,了解更多相关内容。
点击了解:仿生细胞共培养系统
点击了解:仿血流多细胞动态共培养系统
http://www.naturethink.com/?product/81.html






